铜不能自发的和稀硫酸反应。

根据金属活动顺序表,铜排在氢的后面。不能置换出氢。
2.原电池的原理是化学能转化成电能。
既然这个化学反应不能发生,那就不存在能量的转化,不能产生电能。
自发进行的氧化还原反应才能够设计成原电池。
3.不能自发进行的反应,如果借助外力,就有可能发生。
所以,如果将该反应设计成电解池,接通电源后,在电能的作用下,不能进行的反应得到了外力的帮助,就可以发生反应了。
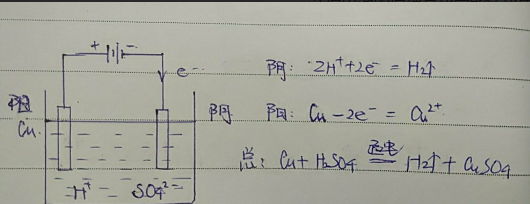
4.不会分析电解池原理?没关系,五句话告诉你怎么回事。
电解池讲的是电子离家出走的故事。

小结
铜与稀硫酸不能自发的反应,因为低能不能生成高能的物质。
但是如果借助外力,比如说电能,低能的物质有了外界能量的帮助,就可以生成高能的物质了。
所以设计成电解池,外界的电能作为能量,提供帮助给帮助铜与稀硫酸反应,从而该反应在电解池作用下能够发生。